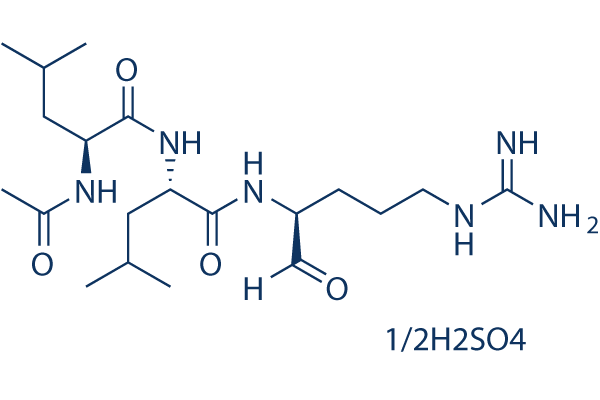
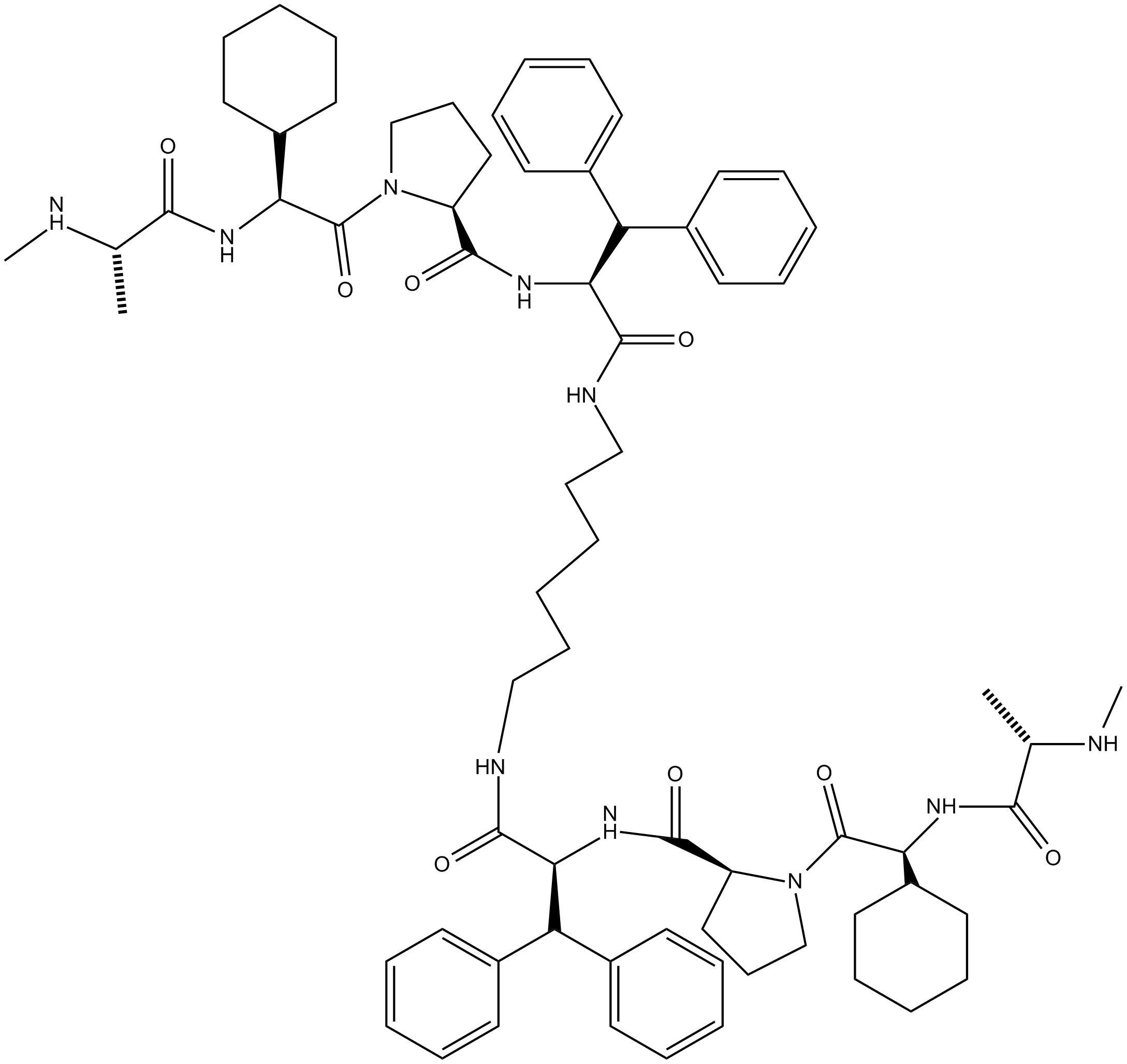
BV6(CAS#1001600-56-1):靶向cIAP1/XIAP的高选择性IAP拮抗剂及其在癌症与子宫内膜异位症中的研究进展
BV6的核心作用机制在于**特异性靶向并促进cIAP1和XIAP蛋白的快速泛素化降解**,从而解除其对caspase级联反应的抑制,最终激活caspase-3依赖性凋亡通路。
在癌症治疗领域,BV6展现出明确的双重靶向优势:对HCC193细胞IC₅₀为7.2 μM;在H460细胞中虽需更高浓度(≥30 μM)方可显著抑制增殖,但其与放疗联用时表现出卓越的放射增敏效应——DER达1.38(p<0.05),证实其可显著提升非小细胞肺癌细胞对电离辐射的敏感性。
进一步机制研究显示:1 μM BV6处理HCC193细胞12小时即可启动caspase-3裂解,48小时内呈时间依赖性增强;而5 μM BV6可在1小时内完全耗竭H460细胞中的cIAP1,并于24小时起下调XIAP表达。
在子宫内膜异位症研究中,BV6同样展现突破性潜力。在雌二醇诱导的BALB/c小鼠模型中,腹腔注射BV6(10 mg/kg,每周两次,持续4周)后,病变总数由4.6降至2.8个/只、平均病变重量从78.1 mg下降至32.0 mg、表面积减少近55%(44.5 vs. 24.6 mm²);同时Ki67阳性细胞比例显著降低,免疫组化证实cIAP-1、cIAP-2及XIAP蛋白表达强度明显减弱,survivin核定位信号同步下调。
拓展应用方向包括:增强CIK细胞对H9、THP-1等血液瘤及RH1、RH30等实体瘤的杀伤能力;在树突细胞中适度激活NF-κB通路,提示潜在免疫调节功能;与TNFα中和抗体(如英夫利昔单抗)联用可协同调控细胞命运决定平衡。
值得注意的是,BV6为**仅供科学研究使用**,不可用于人体或动物临床治疗。所有实验均需严格遵循细胞活力检测(CellTiter 96®)、MTS/PMS法及标准化动物给药方案。其溶解度换算表支持精准剂量配置:例如配制10 mM BV6溶液,10 mg样品仅需0.8295 mL DMSO。
参考文献涵盖《Journal of Thoracic Oncology》(2011)与《Human Reproduction》(2015)等权威期刊,为BV6的转化医学研究提供坚实依据。































请先 登录后发表评论 ~